Giải Khoa học tự nhiên 8 sách Kết nối tri thức, bài 3: Mol và tỉ khối chất khí
Giải Khoa học tự nhiên 8 sách Kết nối tri thức, bài 3: Mol và tỉ khối chất khí - Trang 16, 17,18, 19.
* Mở đầu
Bằng phép đo thông thường, ta chỉ xác định được khối lượng chất rắn, chất lỏng hoặc thể tích của chất khí. Làm thế nào để biết lượng chất có bao nhiêu phân tử, nguyên tử?
Trả lời:
Để biết được lượng chất có bao nhiêu phân tử, nguyên tử ta cần sử dụng khái niệm mol.
Trả lời:
Để biết được lượng chất có bao nhiêu phân tử, nguyên tử ta cần sử dụng khái niệm mol.
I. Mol
Câu hỏi 1 - Trang 17: Đọc thông tin Hình 3.1 và so sánh khối lượng của 1 mol nguyên tử carbon, 1 mol phân tử iodine và 1 mol phân tử nước.
Trả lời:
+ Khối lượng 1 mol nguyên tử carbon là 12 gam.
+ Khối lượng 1 mol phân tử iodine là 254 gam.
+ Khối lượng 1 mol phân tử nước là 18 gam.
Vậy khối lượng 1 mol nguyên tử carbon < khối lượng 1 mol phân tử nước < khối lượng 1 mol phân tử iodine.
Câu hỏi 2 - Trang 17: Tính số nguyên tử, phân tử có trong mỗi lượng chất sau:
a) 0,25 mol nguyên tử C;
b) 0,002 mol phân tử I2;
c) 2 mol phân tử H2O.
Trả lời:
Ta có mol là lượng chất có chứa NA (6,022 × 1023) nguyên tử hoặc phân tử của chất đó. Vậy:
a) 0,25 mol nguyên tử C có 0,25 × 6,022 × 1023 = 1,5055 × 1023 nguyên tử C.
b) 0,002 mol phân tử I2 có 0,002 × 6,022 × 1023 = 1,2044 × 1021 phân tử I2.
c) 2 mol phân tử H2O có 2 × 6,022 × 1023 = 1,2044 × 1024 phân tử H2O.
Câu hỏi 3 - Trang 17: Một lượng chất sau đây tương đương bao nhiêu mol nguyên tử hoặc mol phân tử?
a) 1,2044. 1022 phân tử Fe2O3;
b) 7,5275. 1024 nguyên tử Mg.
Trả lời:
Ta có mol là lượng chất có chứa NA (6,022 × 1023) nguyên tử hoặc phân tử của chất đó. Vậy:
a) 1,2044. 1022 phân tử Fe2O3 tương đương với khoa học tự nhiên = 0,02 mol phân tử Fe2O3.
= 0,02 mol phân tử Fe2O3.
b) 7,5275. 1024 nguyên tử Mg tương đương với khoa học tự nhiên = 12,5 mol nguyên tử Mg.
= 12,5 mol nguyên tử Mg.
Trả lời:
+ Khối lượng 1 mol nguyên tử carbon là 12 gam.
+ Khối lượng 1 mol phân tử iodine là 254 gam.
+ Khối lượng 1 mol phân tử nước là 18 gam.
Vậy khối lượng 1 mol nguyên tử carbon < khối lượng 1 mol phân tử nước < khối lượng 1 mol phân tử iodine.
Câu hỏi 2 - Trang 17: Tính số nguyên tử, phân tử có trong mỗi lượng chất sau:
a) 0,25 mol nguyên tử C;
b) 0,002 mol phân tử I2;
c) 2 mol phân tử H2O.
Trả lời:
Ta có mol là lượng chất có chứa NA (6,022 × 1023) nguyên tử hoặc phân tử của chất đó. Vậy:
a) 0,25 mol nguyên tử C có 0,25 × 6,022 × 1023 = 1,5055 × 1023 nguyên tử C.
b) 0,002 mol phân tử I2 có 0,002 × 6,022 × 1023 = 1,2044 × 1021 phân tử I2.
c) 2 mol phân tử H2O có 2 × 6,022 × 1023 = 1,2044 × 1024 phân tử H2O.
Câu hỏi 3 - Trang 17: Một lượng chất sau đây tương đương bao nhiêu mol nguyên tử hoặc mol phân tử?
a) 1,2044. 1022 phân tử Fe2O3;
b) 7,5275. 1024 nguyên tử Mg.
Trả lời:
Ta có mol là lượng chất có chứa NA (6,022 × 1023) nguyên tử hoặc phân tử của chất đó. Vậy:
a) 1,2044. 1022 phân tử Fe2O3 tương đương với khoa học tự nhiên
b) 7,5275. 1024 nguyên tử Mg tương đương với khoa học tự nhiên
2. Khối lượng mol
Câu hỏi 1 - Trang 18: Tính khối lượng mol của chất X, biết rằng 0,4 mol chất này có khối lượng 23,4 gam.
Trả lời:
Khối lượng mol của chất X là:
Áp dụng công thức: M = =
= 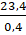 = 58,5 (g/mol)
= 58,5 (g/mol)
Câu hỏi 2 - Trang 18: Tính số mol phân tử có trong 9 gam nước, biết rằng khối lượng mol của nước là 18 g/ mol.
Trả lời:
Số mol phân tử có trong 9 gam nước là:
Áp dụng công thức:
M = => n =
=> n = 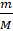 =
= 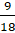 = 0,5 (mol)
= 0,5 (mol)
Câu hỏi 3 - Trang 18: Calcium carbonate có công thức hóa học là CaCO3
a) Tính khối lượng phân tử của calcium carbonate.
b) Tính khối lượng của 0,2 mol calcium carbonate.
Trả lời:
a) Khối lượng phân tử của calcium carbonate:
40 + 12 + 16 × 3 = 100 (amu).
b) Khối lượng của 0,2 mol calcium carbonate là:
Áp dụng công thức:
M = => m = M x n = 100 x 0,2 = 20 (gam)
=> m = M x n = 100 x 0,2 = 20 (gam)
Trả lời:
Khối lượng mol của chất X là:
Áp dụng công thức: M =
Câu hỏi 2 - Trang 18: Tính số mol phân tử có trong 9 gam nước, biết rằng khối lượng mol của nước là 18 g/ mol.
Trả lời:
Số mol phân tử có trong 9 gam nước là:
Áp dụng công thức:
M =
Câu hỏi 3 - Trang 18: Calcium carbonate có công thức hóa học là CaCO3
a) Tính khối lượng phân tử của calcium carbonate.
b) Tính khối lượng của 0,2 mol calcium carbonate.
Trả lời:
a) Khối lượng phân tử của calcium carbonate:
40 + 12 + 16 × 3 = 100 (amu).
b) Khối lượng của 0,2 mol calcium carbonate là:
Áp dụng công thức:
M =
3. Thể tích mol của chất khí
Câu hỏi 1 -Trang 18: Ở 25oC và 1 bar, 1,5 mol khí chiếm thể tích bao nhiêu?
Trả lời:
Ở điều kiện chuẩn (25oC và 1 bar), 1 mol khí bất kì đều chiếm thể tích là 24,79 lít.
Vậy 1,5 mol khí ở điều kiện này chiếm thể tích V = 1,5 × 24,79 = 37,185 lít.
Câu hỏi 2 - Trang 18: Một hỗn hợp khí gồm 1 mol khí oxygen với 4 mol khí nitrogen. Ở 25oC và 1 bar, hỗn hợp này có thể tích là bao nhiêu?
Trả lời:
Tổng số mol khí trong hỗn hợp là: 1 + 4 = 5 (mol).
Ở điều kiện chuẩn (25oC và 1 bar), 1 mol khí bất kì đều chiếm thể tích là 24,79 lít.
Vậy 5 mol hỗn hợp khí ở điều kiện này chiếm thể tích:
V = 5 × 24,79 = 123,95 (lít).
Câu hỏi 3 - Trang 18: Tính số mol khí chứa trong bình có thể tích 500 mililít ở 25oC và 1 bar.
Trả lời:
Ở điều kiện chuẩn (25oC và 1 bar), 1 mol khí bất kì đều chiếm thể tích là 24,79 lít.
Đổi 500 mililít = 0,5 lít.
Số mol khí chứa trong bình có thể tích 0,5 lít ở điều kiện chuẩn là:
Áp dụng công thức: V = n × 24,79
n =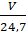 =
= 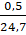
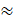 0,02 (mol)
0,02 (mol)
Trả lời:
Ở điều kiện chuẩn (25oC và 1 bar), 1 mol khí bất kì đều chiếm thể tích là 24,79 lít.
Vậy 1,5 mol khí ở điều kiện này chiếm thể tích V = 1,5 × 24,79 = 37,185 lít.
Câu hỏi 2 - Trang 18: Một hỗn hợp khí gồm 1 mol khí oxygen với 4 mol khí nitrogen. Ở 25oC và 1 bar, hỗn hợp này có thể tích là bao nhiêu?
Trả lời:
Tổng số mol khí trong hỗn hợp là: 1 + 4 = 5 (mol).
Ở điều kiện chuẩn (25oC và 1 bar), 1 mol khí bất kì đều chiếm thể tích là 24,79 lít.
Vậy 5 mol hỗn hợp khí ở điều kiện này chiếm thể tích:
V = 5 × 24,79 = 123,95 (lít).
Câu hỏi 3 - Trang 18: Tính số mol khí chứa trong bình có thể tích 500 mililít ở 25oC và 1 bar.
Trả lời:
Ở điều kiện chuẩn (25oC và 1 bar), 1 mol khí bất kì đều chiếm thể tích là 24,79 lít.
Đổi 500 mililít = 0,5 lít.
Số mol khí chứa trong bình có thể tích 0,5 lít ở điều kiện chuẩn là:
Áp dụng công thức: V = n × 24,79
n =
II. TỈ KHỐI CHẤT KHÍ
Câu hỏi 1 - Trang 19:
a) Khí carbon dioxide (CO2) nặng hay nhẹ hơn không khí bao nhiêu lần?
b) Trong lòng hang sâu thường xảy ra quá trình phân hủy chất vô cơ hoặc hữu cơ, sinh ra khí carbon dioxide. Hãy cho biết khí carbon dioxide tích tụ ở trên nền hang hay bị không khí đẩy bay lên trên.
Trả lời:
a) Khối lượng mol của khí carbon dioxide (CO2)bằng 12 + 16.2 = 44 (g/mol)
Tỉ khối của khí carbon dioxide (CO2) đối với không khí bằng dCO2/kk =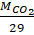 =
= 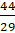 = 1,52 (mol)
= 1,52 (mol)
Vậy khí carbon dioxide (CO2) nặng hơn không khí 1,52 lần
b) Trong lòng hang sâu thường xảy ra quá trình phân huỷ chất vô cơ hoặc hữu cơ, sinh ra khí carbon đioxide. Khí carbon đioxide tích tụ ở trên nền hang do khí đó nặng hơn không khí.ơ
Câu hỏi 2 - Trang 19:
a) Khí methane (CH4) nặng hơn hay nhẹ hơn không khí bao nhiêu lần?
b) Dưới đáy giếng thường xảy ra quá trình phân huỷ chất hữu cơ, sinh ra khí methane. Hãy cho biết khí methane tích tụ dưới đáy giếng hay bị không khí đẩy bay lên trên.
Trả lời:
a) Khối lượng phân tử khí methane: 12 + 4 . 1 = 16 (amu).
Tỉ khối của khí methane so với không khí: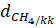 =
=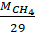 =
=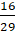
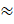 0,55
0,55
Vậy khí methane nhẹ hơn không khí khoảng 0,55 lần.
b) Dưới đáy giếng thường xảy ra quá trình phân huỷ chất hữu cơ, sinh ra khí methane. Do nhẹ hơn không khí nên khí methane sẽ không tích tụ dưới đáy giếng mà bị không khí đẩy bay lên trên.
Em có thể trang 19: Cảnh báo nguy cơ mất an toàn khi nạo, vét giếng, thám hiểm hang, động ….
Trả lời:
Các giếng nước hay hang động, hầm lò sâu… thường có nhiều khí độc tích tụ như CO2; H2S… Hàng năm, nước ta có rất nhiều vụ tử vong thương tâm do ngạt khí khi nạo vét giếng… Do vậy, đối với những giếng nước, hang động, hầm lò sâu chúng ta luôn phải cảnh giác, trước khi đưa người xuống cần phải thăm dò xem không khí dưới đó có thở được không.
Ví dụ một số cách thử trước khi xuống nạo, vét giếng như:
+ Thắp một ngọn nến, dòng dây thả dần sát xuống mặt nước nếu ngọn nến vẫn cháy sáng bình thường là không khí dưới đáy giếng có đủ oxygen, người có thể xuống được. Nếu ngọn nến chỉ cháy leo lét rồi tắt thì không nên xuống vì dưới đó thiếu oxygen hoặc phải trang bị bình dưỡng khí trước khi xuống.
+ Nhốt một con vật vào lồng, buộc dây thả gần sát mặt giếng, nếu con vật bị chết ngạt chứng tỏ không khí dưới đáy giếng thiếu oxygen …
a) Khí carbon dioxide (CO2) nặng hay nhẹ hơn không khí bao nhiêu lần?
b) Trong lòng hang sâu thường xảy ra quá trình phân hủy chất vô cơ hoặc hữu cơ, sinh ra khí carbon dioxide. Hãy cho biết khí carbon dioxide tích tụ ở trên nền hang hay bị không khí đẩy bay lên trên.
Trả lời:
a) Khối lượng mol của khí carbon dioxide (CO2)bằng 12 + 16.2 = 44 (g/mol)
Tỉ khối của khí carbon dioxide (CO2) đối với không khí bằng dCO2/kk =
Vậy khí carbon dioxide (CO2) nặng hơn không khí 1,52 lần
b) Trong lòng hang sâu thường xảy ra quá trình phân huỷ chất vô cơ hoặc hữu cơ, sinh ra khí carbon đioxide. Khí carbon đioxide tích tụ ở trên nền hang do khí đó nặng hơn không khí.ơ
Câu hỏi 2 - Trang 19:
a) Khí methane (CH4) nặng hơn hay nhẹ hơn không khí bao nhiêu lần?
b) Dưới đáy giếng thường xảy ra quá trình phân huỷ chất hữu cơ, sinh ra khí methane. Hãy cho biết khí methane tích tụ dưới đáy giếng hay bị không khí đẩy bay lên trên.
Trả lời:
a) Khối lượng phân tử khí methane: 12 + 4 . 1 = 16 (amu).
Tỉ khối của khí methane so với không khí:
Vậy khí methane nhẹ hơn không khí khoảng 0,55 lần.
b) Dưới đáy giếng thường xảy ra quá trình phân huỷ chất hữu cơ, sinh ra khí methane. Do nhẹ hơn không khí nên khí methane sẽ không tích tụ dưới đáy giếng mà bị không khí đẩy bay lên trên.
Em có thể trang 19: Cảnh báo nguy cơ mất an toàn khi nạo, vét giếng, thám hiểm hang, động ….
Trả lời:
Các giếng nước hay hang động, hầm lò sâu… thường có nhiều khí độc tích tụ như CO2; H2S… Hàng năm, nước ta có rất nhiều vụ tử vong thương tâm do ngạt khí khi nạo vét giếng… Do vậy, đối với những giếng nước, hang động, hầm lò sâu chúng ta luôn phải cảnh giác, trước khi đưa người xuống cần phải thăm dò xem không khí dưới đó có thở được không.
Ví dụ một số cách thử trước khi xuống nạo, vét giếng như:
+ Thắp một ngọn nến, dòng dây thả dần sát xuống mặt nước nếu ngọn nến vẫn cháy sáng bình thường là không khí dưới đáy giếng có đủ oxygen, người có thể xuống được. Nếu ngọn nến chỉ cháy leo lét rồi tắt thì không nên xuống vì dưới đó thiếu oxygen hoặc phải trang bị bình dưỡng khí trước khi xuống.
+ Nhốt một con vật vào lồng, buộc dây thả gần sát mặt giếng, nếu con vật bị chết ngạt chứng tỏ không khí dưới đáy giếng thiếu oxygen …
Ý kiến bạn đọc
Theo dòng sự kiện
Những tin mới hơn
Những tin cũ hơn
DANH MỤC
Bài học mới
-
 Hãy viết bài văn nghị luận bàn về lối sống phông bạt của giới trẻ hiện nay
Hãy viết bài văn nghị luận bàn về lối sống phông bạt của giới trẻ hiện nay
-
 Đề kiểm tra cuối học kì 1, môn: Tin học 6 Kết nối tri thức
Đề kiểm tra cuối học kì 1, môn: Tin học 6 Kết nối tri thức
-
 Đề kiểm tra giữa học kì 1, môn: Giáo dục công dân 6 Kết nối tri thức
Đề kiểm tra giữa học kì 1, môn: Giáo dục công dân 6 Kết nối tri thức
-
 Đề thi tham khảo môn Ngữ Văn, kỳ thi đánh giá năng lực xét tuyển đại học hệ chính quy năm 2025
Đề thi tham khảo môn Ngữ Văn, kỳ thi đánh giá năng lực xét tuyển đại học hệ chính quy năm 2025
-
 Đề thi tham khảo môn Toán, kỳ thi đánh giá năng lực xét tuyển đại học hệ chính quy năm 2025
Đề thi tham khảo môn Toán, kỳ thi đánh giá năng lực xét tuyển đại học hệ chính quy năm 2025
-
 Đề thi tham khảo môn Tiếng Anh, kỳ thi đánh giá năng lực xét tuyển đại học hệ chính quy năm 2025
Đề thi tham khảo môn Tiếng Anh, kỳ thi đánh giá năng lực xét tuyển đại học hệ chính quy năm 2025